近日,至尊国际 教授孔望清、特聘副研究员平媛媛团队在Journal of the American Chemical Society(《美国化学会志》)发表了题为“Direct and Enantioselective Acylation of Diverse C(sp3)–H Bonds with Aldehydes ”的研究成果。该工作报道了一种光促氢原子转移(HAT)与镍催化协同策略,在温和条件下实现了手性α-取代酮化合物的高效合成。至尊国际 博士后周志俊、硕士生胡芬为论文共同第一作者,孔望清与平媛媛为论文通讯作者,至尊国际 为第一署名单位。

具有α-芳基、α-氨基或α-氧代叔碳立体中心的手性酮,是多种重要天然产物和药物中的独特结构单元。同时,该类化合物也是合成二醇、氨基醇等重要手性中间体的通用前体,尤其适用于构建含连续手性中心的手性结构。尽管手性α‑取代酮在药物化学领域具有重要价值,但其高效、高对映选择性的合成方法仍面临诸多挑战。孔望清研究团队系统性开展了氢原子转移(HAT)与金属协同催化实现C(sp3)–H键立体选择性官能化的相关研究,并取得系列重要突破。在2023年通过光促HAT/镍协同催化的策略,该团队成功实现了氧杂环C(sp3)–H键对映选择性芳基化和烯基化反应(J. Am. Chem. Soc.2023,145, 5231–5241.)。随后,该团队创新性地开发了氧化氢原子转移与还原偶联协同催化体系,率先实现了饱和杂环化合物的不对称C(sp3)−H烷基化反应(Nat. Chem.2025,17, 344–355.),该反应避免贵金属的使用,还解决了缺乏导向基团的饱和烃对映选择性构建C(sp3)–C(sp3)键的困难。在先前工作研究基础之上(Acc. Chem. Res.2025,58, 2477–2495.),该团队从稳定易得的醛类底物出发,利用光能量转移活化过氧化物,实现两类不同碳氢键的不对称交叉脱氢偶联(CDC),高效完成α-取代酮的对映选择性合成。值得提出的是:经典CDC反应中,过氧化物的使用通常需要加热(90 ℃)以促进其均裂产生烷氧基自由基;而光能量转移可在较低温度(0–25 ℃)下实现过氧化物的均裂,这可能是能够实现立体选择性控制的关键。
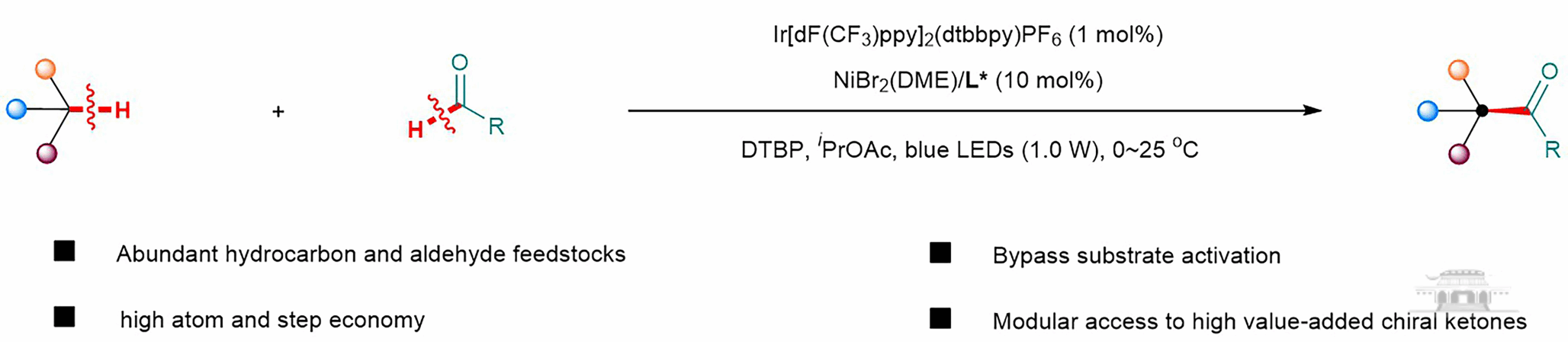
该研究为多种C(sp3)−H键的立体选择性酰基化提供了高效合成策略。以来源丰富、易于获取的醛作为酰基源,可实现苄位、α-氨基及氧α-位等多种C(sp3)−H键的直接酰基化转化,有效解决了传统酰基化试剂需预先制备、稳定性不佳等关键问题。此外,该方法的合成应用价值已在天然产物及药物相关分子的不对称合成中得到充分验证。
该研究工作得到了国家自然科学基金、南京大学化学化工学院配位化学国家重点实验室开放研究基金、江苏省基础研究计划资助、广东省基础与应用基础研究基金以及中国博士后科学基金的经费支持。感谢至尊国际 科研公共服务条件平台对本研究的支持。
论文链接://pubs.acs.org/doi/10.1021/jacs.5c18382
新闻链接://news.zzunguoji.com/info/1015/491767.htm



 武大主页
武大主页 武大邮箱
武大邮箱 信息门户
信息门户 English
English